基因敲除服务价格-博天堂备用
价格: 询价
产品详情
文献和实验
商家信息
相关推荐
crispr/cas(clustered regularly interspaced short palindromic repeats/cas)系统是目前被广泛运用的基因编辑系统,其原理是由crispr转录产生的grna介导cas核酸酶靶向目标序列,对序列进行切割。其中最常用的是靶向dna的crispr/cas9系统,此系统是由ii类crispr/cas系统改造而来,能够在植物、细菌、酵母、鱼类及哺乳动物等多种细胞中,进行有效的靶向编辑,具有操作简易、效率高、以及作用靶位点多等优势。
crispr/cas9系统中sgrna(short guide rna)识别并结合目标基因的靶向序列,引导cas9对结合位点进行剪切,产生dna双链断裂(double-strand break, dsb),机体自身通过非同源重组(non-homologous end joining,nhej)的方式修复dsb,参与修复的蛋白经常会在dna末端插入或删除几个碱基,修复后的基因由于产生突变而导致功能丧失,从而实现机体内的基因敲除。
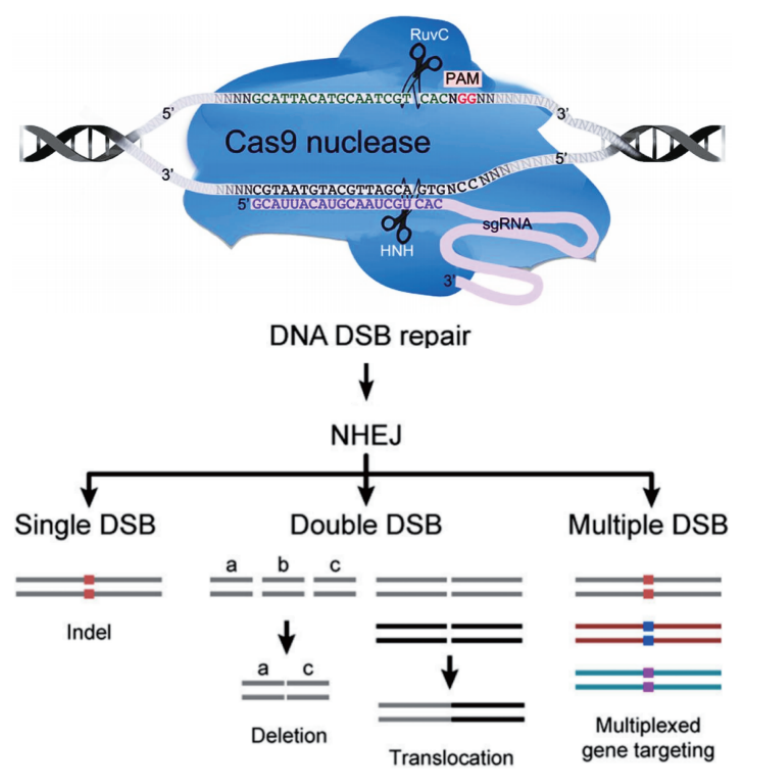
crispr/cas9系统介导的基因编辑(wiles m v et al. mammalian genome, 2015)
应用
1. crispr/cas9基因敲除细胞系建立
2. crispr/cas9基因敲除建立动物疾病模型
技术优势
1. 操作简易:仅需cas9核酸酶和sgrna即可对目标基因靶位点进行切割;
2. 效率高:在基因组水平上编辑目标基因,高度模拟目标模型,可精确编辑基因组;
3. 作用靶位点多:可实现多个靶基因位点及多个基因的同时敲除;
4. 提供多种基因编辑病毒工具:aav、lv;
5. 提供bsl-1和bsl-2病毒注射及实验操作平台;
6. 全面的实验博天堂备用的技术支持。
服务内容
1. sgrna的设计;
2. 细胞内sgrna剪切活性筛选;
3. 敲除载体的构建;
4. 依据所要编辑的细胞选择cas9和sgrna不同导入方式:
a、脂质体易转染细胞:使用质粒系统(cas9和sgrna);
b、 脂质体难转染细胞:使用质粒系统电转化、慢病毒或腺相关病毒感染(cas9和sgrna);
5. 筛选基因敲除单克隆细胞系。
服务流程
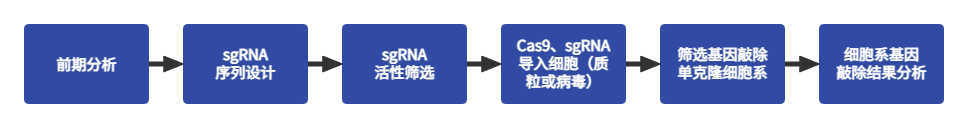
客户提供
1. 目的基因基因序列(序列/id)以及物种来源;
2. 需介导基因敲除的细胞(可选);
3. 病毒类型选择以及要求;
4. 血清型选择。
服务信息及最终交付内容、产品
| 流程分布 | 周期 (工作日) |
交付内容 | 交付产品 |
|---|---|---|---|
| sgrna序列的设计 | 2-4周 | sgrna设计分析报告 | - |
| sgrna的活性筛选 | 获得有活性的sgrna及筛选报告 | ||
| 基因敲除质粒的构建 | 1周 | 基因敲除质粒报告 | 基因敲除质粒 |
| 病毒包装 | 3周 | 病毒包装报告 | 高纯度病毒 |
| 单克隆细胞分选 | 8周 | 单克隆细胞分选及检测结果报告 | 基因敲除单克隆细胞系 |
声明:枢密科技提供的所有基因编辑服务及该服务的后续研究,仅适用在国家法律和伦理规范的范围内实施。禁止用于任何人体或临床实验的研究;禁止用于对人类生殖体系进行基因修饰的研究;禁止将基因修饰的其他动物胚胎及生殖细胞植入人体。客户如违反相关法律规定,本公司不承担任何法律责任。
案例展示
haoyi wang等人研究发现,crispr / cas介导的基因编辑允许高效地同时破坏小鼠胚胎干(es)细胞中的五个基因(tet1,2,3,sry,uty-8等位基因),通过nhej引入多个随机indel的靶向突变。将靶向tet1和tet2的cas9 mrna和sgrna共注射到受精卵中,在两种基因中产生具有双等位基因突变的小鼠,效率为80%。crispr / cas系统允许一步产生携带多个基因突变的动物,这种方法将大大加速功能冗余基因和上位基因相互作用的体内研究。
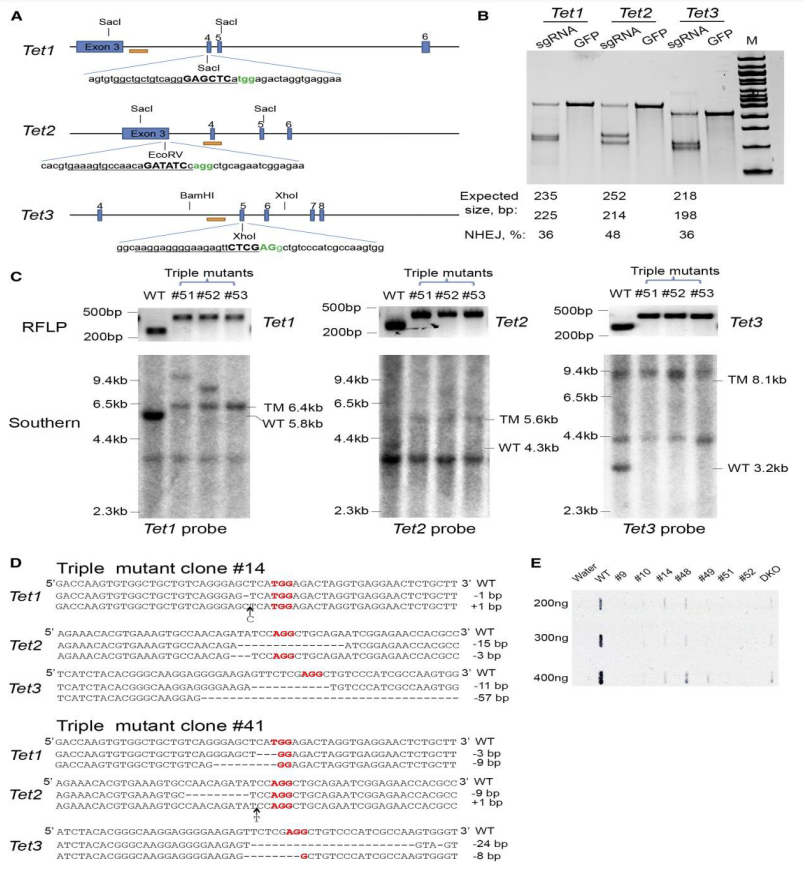
小鼠胚胎干细胞的多基因敲除(wang h et al. cell, 2013)
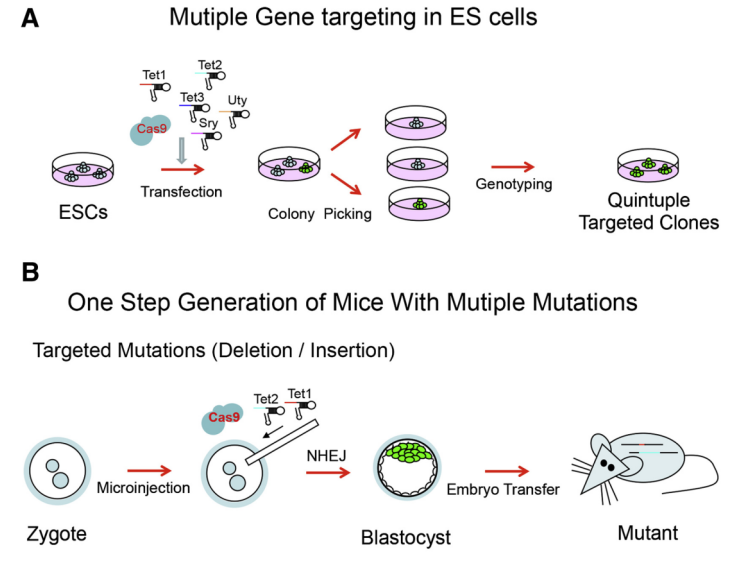
小鼠和小鼠胚胎干细胞的多基因编辑(wang h et al. cell, 2013)
参考文献
1. wiles m v , qin w , cheng a w , et al. crispr–cas9-mediated genome editing and guide rna design[j]. mammalian genome, 2015, 26(9-10).
2. wang h , yang h , shivalila c , et al. one-step generation of mice carrying mutations in multiple genes by crispr/cas-mediated genome engineering[j]. cell, 2013, 153(4):910-918.
联系人:枢先生
地址:武汉